
La vacuna de Pfizer y BioNTech, uno de los diez proyectos en todo el mundo que están más cerca de lograr la aprobación, podría lograr una efectividad del 90%, según anunciaron ambas farmacéuticas este lunes. La noticia tuvo una enorme repercusión mundial que se reflejó también en las bolsas, y algunos gobiernos, como el español, se apresuraron a hablar de fechas y cifras: el ministro de Sanidad, Salvador Illa, apuntó a veinte millones de dosis disponibles entre finales de 2020 y principios de 2021 para vacunar a diez millones de personas.
Aunque se trata de una noticia importante y esperanzadora, reflejo del enorme esfuerzo a nivel mundial que se está haciendo para desarrollar en meses lo que habitualmente cuesta años, aún quedan muchos pasos para que esa, u otra vacuna, esté aprobada, distribuida y lista para ser suministrada, y hay muchas dudas sobre aspectos como la duración de la inmunidad y la respuesta que pueda provocar entre los más vulnerables. Estas son algunas de las claves que aconsejan ser prudente, rebajar la euforia y no bajar la guardia.
Resultado provisional
Pfizer anunció una efectividad del 90% en 94 casos confirmados de covid-19 entre sus más de 40.000 voluntarios, pero las pruebas deben continuar. Los resultados a los que aludió Pfizer en su nota de prensa se referían a un estudio intermedio dentro de los ensayos clínicos de fase 3 (la última y más importante en el desarrollo de una vacuna), que aún debe ser publicado y revisado por pares. Los datos preliminares le permiten comenzar a tramitar la autorización de emergencia de las autoridades estadounidenses. Pero la farmacéutica ha de continuar sus ensayos hasta publicar un análisis final cuando los casos confirmados de covid-19 alcancen la cifra de 164 y haya más evidencias sobre la inmunidad de los pacientes catorce días después de recibir la segunda dosis de la vacuna, que se suministra 14 días después de la primera. Es decir, aunque Pfizer ha conseguido el hito de ser la primera empresa occidental en presentar datos de eficacia que abren la puerta a su distribución, aún faltan varios pasos indispensables y mucha información sobre los resultados.
El profesor de investigación del CSIC Vicente Larraga, del Centro de Investigaciones Biológicas Margarita Salas, avisa en declaraciones a Efe de que lo que han anunciado Pfizer y BioNTech es un "análisis intermedio, un informe que suele avanzar información de los ensayos pero que no contiene datos concluyentes". También pide esperar la investigadora Sonia Zúñiga, que advierte de que hay que ver "en qué quedan" estas noticias "cuando finalice el ensayo". En su opinión, "faltan muchos datos por saber": "No sabemos ni cuánto dura la protección ni la inmunidad que genera la vacuna, qué grupos de edad hay en esos 94 infectados, si ha funcionado la vacuna para proteger de la enfermedad o para proteger de la infección, o si en el grupo de los infectados son todos asintomáticos y casos leves o personas con síntomas más graves... quedan muchas preguntas por responder". En la misma línea, Raúl Ortiz de Lejarazu, profesor de Microbiología, virólogo y consejero científico del Centro Nacional de Gripe de Valladolid, señala a LD que los datos aún tienen que "publicarse en revistas científicas de prestigio tras revisión por pares": "Si los resultados siguen siendo superiores al 60% de efectividad habrá que ver cuáles han sido los end points clínicos principales y secundarios (no es lo mismo un 90% de eficacia en prevenir casos de cualquier tipo que en prevenir hospitalizaciones, o ingresos en UVI o muerte por covid-19)".
Duración de la inmunidad
La vacuna de Pfizer y BioNTech, la BNT162b2, está basada en una tecnología novedosa, denominada de ARN mensajero, nunca utilizada en vacunas. Consiste en inocular en el paciente moléculas de ácido ribonucleico (ARN) iguales a las del virus para que "la célula en la que entre fabrique y produzca la proteína S del SARS-Cov-2", explica a LD Lejarazu. A partir de ahí, se activa la respuesta inmune y el organismo fabrica los anticuerpos para reconocerlo y neutralizarlo. Sólo otra de las diez vacunas que están en la última fase, la de Moderna, utiliza esta modalidad, que tiene la ventaja de que es muy rápida" en su desarrollo pero que entraña limitaciones y desafíos.
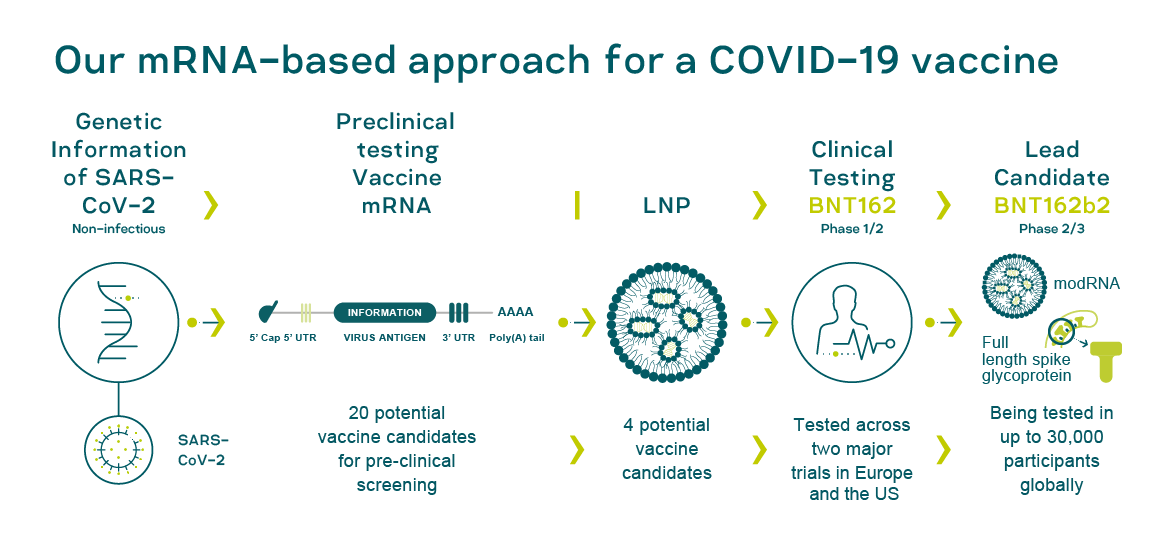
Según explica a LD la inmunóloga Matilde Cañelles, la inmunidad que proporcionan estas vacunas más rápidas, de "primera generación", es "más limitada" que las vacunas basadas en el genoma completo del virus o en virus debilitados. Con las vacunas de la siguiente generación, que sí se basan en el coronavirus completo, "la respuesta inmune, si se produce, va a ser más robusta porque se va a producir contra varias proteínas del virus" y evitas que "el virus pueda mutar" y dicha mutación afecte justo a la proteína en que se basaba tu vacuna. Lejarazu, por su parte, destaca que en cualquier caso la duración del efecto protector, en esta y en el resto de vacunas que se desarrollen, "sólo podrá ser medible a medida que transcurra el tiempo o los ensayos de fase IV". Es y seguirá siendo durante un tiempo una incógnita.
Desafío de la distribución
Uno de los principales inconvenientes de la vacuna de Pfizer y por extensión de las vacunas basadas en el ARN mensajero es la necesidad de utilizar temperaturas extremadamente bajas para conservar las dosis. La vacuna necesita ser manipulada a entre -70 y -80 grados centígrados, lo que supone un desafío logístico de enorme magnitud si lo que se pretende es la vacunación masiva de buena parte de la población mundial. Según explica Cañelles, la razón de que se necesiten estas bajísimas temperaturas es que "el ARN se degrada muy fácilmente". Y aunque se "está buscando la manera de estabilizarlo" y resolver esta cuestión, la necesidad de una vacuna muy rápida ha hecho que no haya habido tiempo de "solucionar este tipo de problemas".
Según Lejarazu, los países que quieran comenzar a inmunizar a su población con esta vacuna tendrán que organizar una logística "muy importante y costosa": "Se estima que para proporcionar una sola dosis a 7,8 millones de personas se podrían necesitar 8.000 aviones Boeing 747 que transportaran los viales a esa temperatura. Y una vez en el país, éste tendría que asumir la seguridad del transporte y no romper la cadena de frío". Para la campaña anual de la gripe, de la que se vacuna en España un 18% de la población, se necesita "un operativo para mantener tres meses una vacuna que se conserva en nevera (+4º)". En el caso de esta vacuna, que se quiere administrar a una proporción de ciudadanos mucho mayor, cabe imaginar las necesidades que se crearán, desde centros de almacenamiento a medios de transporte a los puntos de suministro, sobre los que también hay que decidir y que también deben estar preparados: ¿hospitales? ¿Centros de salud? ¿Instalaciones especiales?

Desde Pfizer, sin embargo, aseguran a LD que van a poner los medios para superar las dificultades: "Hemos desarrollado planes y herramientas logísticas para asegurar un transporte, almacenamiento y control continuo de la temperatura de las vacunas efectivos. Nuestra distribución se basa en un sistema flexible que enviará los viales congelados al punto de vacunación en el momento necesario". Aunque de momento no aportan más detalles, la farmacéutica apunta que intentarán hacer posible que la vacuna llegue convenientemente protegida desde el lugar de fabricación hasta el punto de suministro, pero también avisan de que será imprescindible una importante coordinación con las autoridades de cada país: "Perseguimos trabajar con los gobiernos para apoyar la distribución a quienes se han definido como sus grupos prioritarios y anticipamos que los puntos de vacunación variarán, pero pueden incluir hospitales, centros de salud, lugares de vacunación comunitaria y farmacias".
Desde el Gobierno, el ministro de Ciencia, Pedro Duque, ha señalado que en efecto desde la empresa se ha propuesto "un sistema completo" en el que las dificultades que plantean las temperaturas muy bajas "se incluyen en la oferta que se hace". Según Duque, el Sistema Nacional de Salud podría recibir la vacuna "ya en los sitios adecuados, conservada suficientemente a baja temperatura, de manera que a partir de ahí ya se haga el trabajo normal". Aunque así fuera, el reto es enorme y las necesidades de coordinación y de concreción del plan de vacunación, que Illa quiere tener listo "hacia el 23 de noviembre", también.
Prometer antes de firmar
Varios gobiernos, entre ellos el español, se apresuraron a hablar de fechas y dosis con el contrato aún sin firmar. Salvador Illa prometió poco después de conocerse la noticia las dosis necesarias para vacunar a diez millones de personas y apuntó incluso a la posibilidad de tener vacunas antes de finalizar el año. Pero muchas variables podrían truncar las intenciones del ministro además de las ya comentadas. Otras autoridades, como la Unión Europea, bajo cuyo paraguas llegarán las vacunas a España, se muestran bastante más prudentes. El portavoz de la Comisión Europea, que este miércoles ha dado luz verde a la firma de un contrato conjunto para adquirir 300 millones de dosis, ha avisado de que la vacuna sólo se comprará "una vez se demuestre segura y efectiva contra la covid-19". La Comisión Europea también ha firmado precontrato con otras farmacéuticas con proyectos avanzados: AstraZeneca, Sanofi-GSK y Johnson and Johnson.
Desde Pfizer, mientras, afirman que podrán suministrar 50 millones de dosis para finales de 2020 y "aproximadamente" 1.300 millones a finales de 2021 y que tienen la potencia suficiente como para "fabricar y distribuir rápidamente grandes cantidades" de la vacuna.
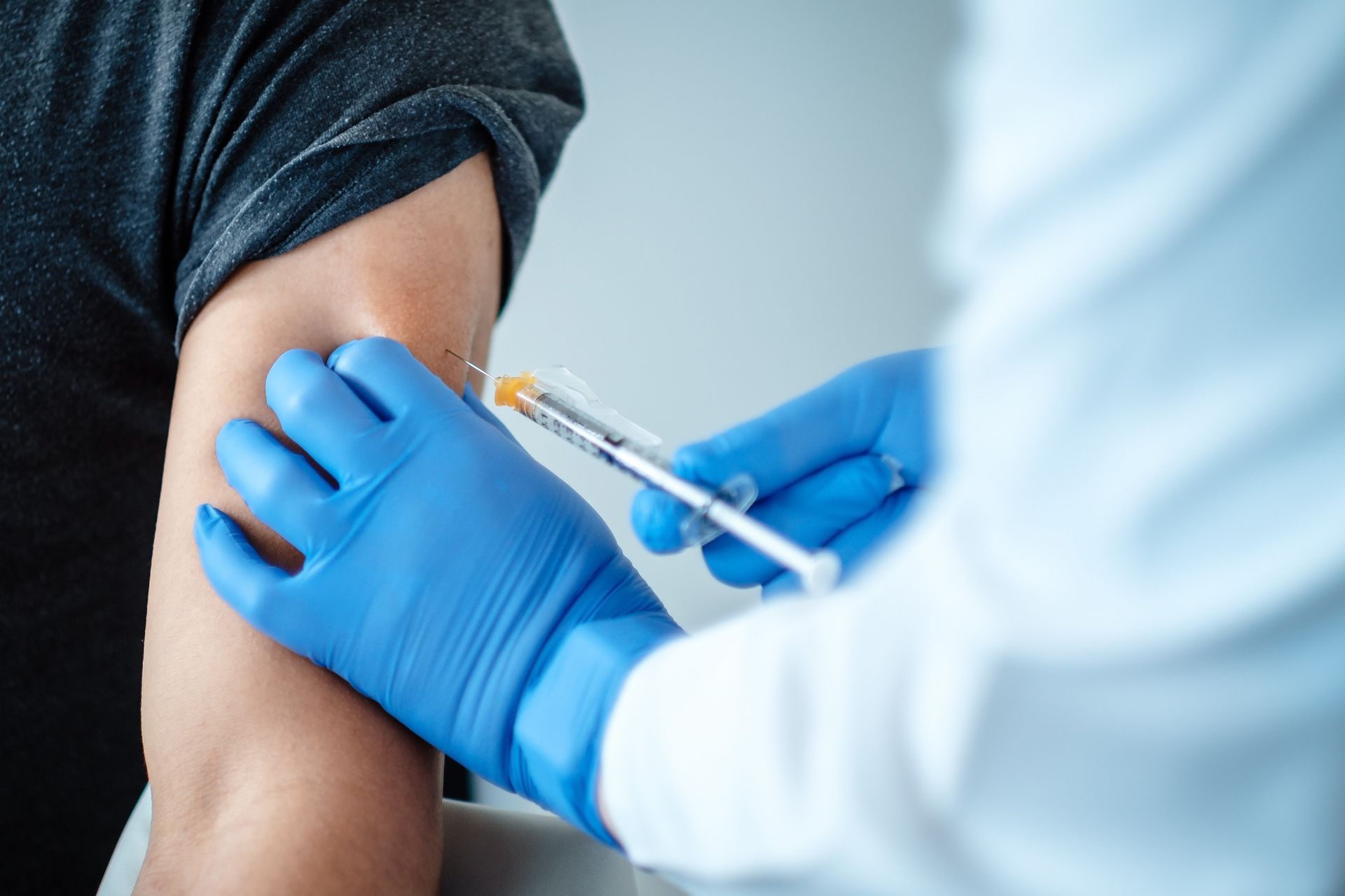
El reto de vacunar
Finalmente, el éxito de la vacuna llegará si se la pone la población a la que va dirigida: sólo así se logrará la ansiada inmunidad de grupo y se reducirán los fallecidos y los ingresos hospitalarios asociados al coronavirus. Si esta vacuna y el resto que están en investigación llegan al mercado, será porque han pasado todos los controles, es decir, serán vacunas seguras. Pero también en este punto queda mucho por hacer: según un estudio de Ipsos realizado en colaboración con el Foro Económico Mundial en países de todo el mundo, seis de cada diez españoles preferiría esperar un año para vacunarse de la covid-19 por las reticencias que les genera la rapidez en su desarrollo y sólo un 13% lo haría inmediatamente. Según indicó hace unos días Illa, la intención del Gobierno es que la vacunación no sea obligatoria, como se está planteando en otros países. Pero para que la mayoría de españolas accedan a ponérsela tendrán que hacer una intensa labor informativa y generar confianza.

